Рак яичников: симптомы и варианты лечения
Как часто встречается рак яичников?
Рак яичников занимает 9-е место по заболеваемости и 8-е место по смертности среди злокачественных новообразований у женщин в Российской Федерации.
Рак яичников развивается из клеток, покрывающих яичники снаружи. Далее мы разберем наиболее распространенные виды эпителиальных новообразований яичников.
Что нужно знать о яичниках?
Яичники - парный орган женской репродуктивной системы. Репродуктивная система – это совокупность органов, которые связаны анатомически и отвечают за размножение. Кроме яичников эта система включает маточные трубы, тело матки, шейку матки и влагалище.
Яичники расположены в малом тазу. Малый таз – это область несколько ниже пупка между тазовыми костями. Один яичник находится с левой стороны от матки, а другой – справа. Каждый яичник соединяется с маткой длинной тонкой трубкой – маточной трубой.
Яичники производят яйцеклетки, а также гормоны, которые влияют на рост молочных желез, телосложение и менструальный цикл. Яйцеклетки выходят из яичника и проходят через маточную трубу в матку, где после оплодотворения растет и развивается плод во время беременности. Матка и хотя бы один яичник необходимы для регулярного менструального цикла и естественного зачатия ребенка (беременности).
Почему возникает рак яичников?
Есть два факта, которые важно усвоить:
- Факторы риска увеличивают вероятность развития рака, но их наличие не означает, что человек обязательно им заболеет.
- Отсутствие факторов риска не означает, что человек НЕ заболеет раком.
Точная причина рака яичников, как и многих злокачественных опухолей, неизвестна. Однако многолетние исследования позволяют выделить несколько ключевых факторов развития заболевания.
Повышают риск рака яичников:
- Раннее наступление и позднее завершение менструаций;
- Отсутствие родов и грудного вскармливания;
- Ожирение;
- Наличие «семейной истории», а именно мутаций в так называемых «генах рака молочной железы» BRCA 1 и BRCA 2, а также синдром Линча;
- Некоторые профессиональные вредности.
Снижают риск рака яичников:
- Прием оральных контрацептивов (по назначению врача);
- Грудное вскармливание;
- Правильное сбалансированное питание (употребление фруктов, овощей, молочных продуктов, рыбы, белого мяса и растительных масел);
- Регулярная физическая активность.
Семейный анамнез играет крайне важную роль в потенциальной возможности возникновения рака яичников. Поэтому советуем обратить внимание на следующие ситуации:
— Несколько случаев одинаковых злокачественных опухолей в семье (например рак яичников и/или молочной железы у бабушки, мамы, дочери);
—Больше одной опухоли у родственника (например, сочетание рака молочной железы и рака яичников);
—Опухоли, нехарактерные для пола пациента (например, рак молочной железы у мужчин).
Важно помнить, что женщины, у которых есть родственники первой линии (мать или дочь), больные раком яичников, более чем в 2 раза чаще подвержены риску этого заболевания [2]. Кроме этого, у таких пациентов болезнь проявляется примерно на 10 лет раньше.
Рак яичников составляет более 90% всех злокачественных опухолей этого органа.
Скрининга рака яичников не существует.
Как исключить заболевание?
Есть несколько простых рекомендаций, которые стоит соблюдать для мониторинга состояния женского здоровья:
— Посещать гинеколога минимум 1 раз в 6-12 месяцев;
— Делать УЗИ органов малого таза не реже 1 раза в год;
— При подозрении на объемные образования яичников сдать кровь для определения СА125, НЕ4, индекса ROMA.
Диагностика рака яичников
Диагностика рака яичников состоит из беседы с врачом, который выясняет историю начала заболевания, собирает жалобы и проводит осмотр. Врач может заподозрить злокачественную опухоль, но чтобы подтвердить диагноз, разобраться в том, какая именно опухоль имеется у пациентки, необходимо дообследование. Дообследование будет включать как лабораторные анализы, так и инструментальные методы.
Специфические лабораторные исследования чаще всего включают в себя анализы крови на онкомаркеры.
Онкомаркер – это вещество, обнаруженное в ткани или жидкости организма, которое может быть признаком злокачественного новообразования. В совокупности с другими данными и анализами онкомаркеры помогают диагностировать, в частности, рак яичников. Также их используют для мониторинга результатов лечения.
Определение СА-125 (CA – cancer antigen, или раковый антиген) – наиболее широко используемый тест в диагностике рака яичников. СА-125 представляет собой белок, вырабатываемый нормальными клетками и клетками рака яичников. Высокий уровень СА-125 в крови может быть признаком ряда онкологических заболеваний, в том числе рака яичников.
Сам по себе тест CA-125 (изолированное повышение данного маркера) не может диагностировать рак, поскольку существуют заболевания, при которых уровень СА-125 может повышаться. Кроме того, при некоторых вариантах рака яичников уровень CA-125 может быть в норме. Но если врач подозревает рак яичников, он обязательно назначит исследование CA-125 в крови в дополнение к базовым обследованиям. Также это исследование проводят в процессе и после лечения.
Определение HE4 (HE — Human Epididymis protein 4, или человеческий эпидидимальный белок 4) повышает чувствительность и специфичность лабораторной диагностики рака яичников. Его уровень вместе с уровнем CA-125 использует при расчете индекса ROMA. Этот показатель определяется по специальной формуле и позволяет судить о риске серозного рака яичников высокой степени злокачественности.
Могут быть назначены исследования других опухолевых маркеров:
- Ингибина (обычно ингибина В);
- Бета-субъединицы хорионического гонадотропина человека (β-ХГЧ);
- Альфа-фетопротеина (АФП);
- Лактатдегидрогеназы (ЛДГ);
- Раково-эмбрионального антигена (СЕА);
- СА-19-9.
Повышение уровней этих маркеров наблюдается при редких вариантах рака яичников и неэпителиальных злокачественных опухолях яичников.
Инструментальные методы диагностики рака яичников используют для подтверждения диагноза, определения локализации и распространенности опухолевого процесса.
- Ультразвуковое исследование (УЗИ) — базовый метод обследования органов брюшной полости и малого таза. Для УЗИ брюшной полости используют наружные датчики. Исследование позволяет оценить наличие жидкости в животе (асцит), изменения в других органах брюшной полости и забрюшинного пространства (печень, селезенка, почки, поджелудочная железа). УЗИ малого таза обычно проводят влагалищным датчиком. При этом визуализируют матку с придатками (придатками называют яичники и маточные трубы), жидкость в малом тазу, изменение размеров и формы яичников. Совокупность ультразвуковых симптомов помогает врачу предположить наличие заболевания яичников.
- При компьютерной томографии (КТ) в вену пациента вводят йодсодержащее контрастное вещество. КТ четко показывает изменения в органах малого таза, в том числе в яичниках, распространение процесса по брюшной и грудной полости, лимфатическим узлам. КТ, как и любое исследование, имеет ограничения, поэтому не всегда выявляет мелкие опухолевые очаги.
- Магнитно-резонансную томографию (МРТ) органов брюшной полости и малого таза, как и КТ, применяют для оценки распространенности рака яичников. Это исследование при подозрении на рак яичников также всегда проводят с контрастным веществом (в отличие от КТ контрастное вещество для МРТ не содержит йод). МРТ дороже и занимает больше времени, чем КТ, но может быть более информативно при раке яичников ранних стадий, а также при подозрении на метастазы в таких органах, как печень.
- Позитронно-эмиссионную томографию (ПЭТ) обычно сочетают с КТ с контрастированием. В этом случае данные о распределении радиофармпрепарата совмещают с изображениями, полученными при КТ, что повышает информативность исследования. ПЭТ-КТ с контрастированием — очень информативный современный метод диагностики. За счет контрастного вещества и радиоактивного изотопа, которые накапливаются в пораженных новообразованиями органах ПЭТ-КТ помогает с высокой долей уверенности оценить распространенность злокачественной опухоли. ПЭТ-КТ может диагностировать те очаги, которые невозможно выявить при УЗИ, КТ или МРТ. Однако этот метод не универсален, так же, как и предыдущие, имеет свои ограничения, и должен применяться по показаниям.
Только высококвалифицированный онкогинеколог может грамотно и своевременно определить какие методы обследования необходимы пациентке и в какой последовательности.
Гистологические типы злокачественных опухолей яичников
Злокачественные эпителиальные опухоли яичников, или рак яичников, наблюдаются чаще неэпителиальных. Выделяют несколько вариантов рака яичников. Чаще всего встречаются:
- Серозный рак (низкой и высокой степени злокачественности);
- Эндометриоидный рак.
Реже встречаются:
- Муцинозный рак;
- Светлоклеточный рак;
- Недифференцированный рак;
- Карциносаркома.
Пограничные опухоли, или опухоли с низким злокачественным потенциалом, занимают промежуточное положение между доброкачественными опухолями и раком яичников.
К неэпителиальным опухолям яичников относятся герминогенные опухоли, а также опухоли стромы полового тяжа.
Как определить стадию рака яичников и прогноз?
Гистологический тип опухоли определяют по результатам гистологического исследования. Для него нужна ткань опухоли, полученная во время операции или при биопсии. Исследование проводит патолог, который и определяет гистологический тип опухоли и степень ее злокачественности (не путайте со стадией!).
Степень злокачественности определяется под микроскопом с учетом выраженности изменений опухолевых клеток. Этот показатель позволяет судить о поведении опухоли. Так, опухоли высокой степени злокачественности растут и распространяются быстрее, чем опухоли низкой степени злокачественности.
Стадию рака яичников определяет хирург после операции. При этом учитывают данные лучевых методов диагностики, находки во время операции и результаты гистологического исследования.
Стадия рака яичников, гистологический тип опухоли и степень злокачественности являются важными, но не единственными факторами, определяющими прогноз рака яичников.
Как правило рак яичников прогрессирует достаточно быстро. При подозрении на рак яичников нельзя терять драгоценное время. Тщательное планирование обследований с целью решения вопроса о тактике и плане лечения должно сопровождаться началом поддерживающей терапии для подготовки к специфическому противоопухолевому лечению.
Лечение рака яичников
Суть лечения рака яичников можно описать следующим образом — уничтожить или уменьшить опухолевую массу. Для этого применяют два метода: хирургический и лекарственный. Лучевую терапию для лечения рака яичников в настоящее время не используют.
Химиотерапия не может уничтожить опухолевые клетки полностью, поэтому мировое врачебное сообщество определило, что хирургическое вмешательство является неотъемлемой составляющей лечения рака яичников.
Первым и определяющим этапом в лечении рака яичников является циторедуктивная операция. К исключениям относят:
- случаи, когда тяжелые сопутствующие заболевания не позволяют провести операцию;
- опухолевый процесс имеет большую распространенность (неоперабелен);
- компетенции хирурга или клиники не позволяют провести операцию.
Хирургия рака яичников – это большая сложная абдоминальная онкохирургия, ведь опухолевые узлы могут выявляться где угодно от малого таза до диафрагмы. Опухолевые диссеминаты зачастую располагаются в труднодоступных местах (вокруг чревного ствола, печени, селезенки, в кардиодиафрагмальных лимфоузлах), то есть поражение при раке яичников поздних стадий охватывает все анатомические зоны брюшной полости. Удаление всех опухолевых узлов подразумевает долгие, кропотливые и травматичные операции. Однако только такие вмешательства приводят к хорошим результатам.
Основная задача онкохирурга - удалить все видимые образования (макрометастазы). Это залог излечения от грозной болезни при дальнейшей адекватной химиотерапии.
По данным ведущих мировых центров хирургии рака яичников (Memorial Sloan Kettering Cancer Center, MD Anderson, Essen University) частота выполнения полных циторедукций колеблется от 60 до 80%, что связано с анатомическим расположением диссеминатов. В зависимости от объема оставшейся в организме опухолевой ткани циторедуктивные операции можно разделить на:
- полные, когда в процессе операции удалены все видимые очаги болезни;
- оптимальные, когда размер наибольшего очага опухоли не превышает 1 см;
- неоптимальные, когда размер хотя бы одного из оставшихся опухолевых очагов составляет более 1 см.
Такое деление определяет дальнейший прогноз заболевания. Именно наличие и размер остаточных опухолей является наиболее важным фактором прогноза при раке яичников и единственным фактором, на который может повлиять хирург. Наиболее благоприятный прогноз будет при полной циторедукции, когда видимой опухолевой ткани после операции не остается. В этой ситуации химиотерапия окажется наиболее эффективной.
Статистика не только в РФ, но и в мире подтверждает, что единичные хирурги способны успешно провести полную / оптимальную циторедукцию при распространенном раке яичников, поэтому выбирайте хирурга осознанно!
Когда оперироваться: до или после химиотерапии?
Данные из ведущих мировых центров лечения рака яичников указывают, что пациентки живут дольше и лучше, если полная циторедукция проведена до химиотерапии. В этом есть определенная логика: когда масса опухолевых клеток удалена хирургическим путем, с помощью химиотерапии гораздо проще уничтожить микрометастазы. Хирургическое лечение рака яичников, выполняемое на первом этапе с последующей химиотерапией, называют первичной циторедукцией.
Но есть и другой сценарий, когда распространенность болезни не позволяет выполнить полное удаление макрометастазов, вследствие их распространения и/или тяжелого состояния пациентки и/или недостаточной компетенции хирурга. Тогда пациентка проходит 3 курса химиотерапии, чтобы уменьшить количество и размер макрометастазов. В этом случае хирургу проще удалить их вместе с первичной опухолью. Такая операция называется интервальной циторедукцией.
К сожалению, по данным ряда научных исследований, время до прогрессирования и общая продолжительность жизни в группе интервальных циторедукций меньше, чем в группе первичных циторедукций.
Первичная циторедукция – это не просто тактика, а рекомендованная мировым сообществом онкогинекологов практика лечения распространенного рака яичников. На первом этапе выполняется хирургическое удаление всех видимых очагов опухоли. Вторым этапом идет химиотерапия, которая воздействует на невидимые глазом метастазы.
При интервальной циторедукции до хирургического лечения проводится несколько курсов химиотерапии. Стандартом является проведение не более 3 курсов лечения.
Хирургическое лечение рака яичников I–II стадий
Чем раньше диагностирована злокачественная опухоль, тем лучше прогноз. Однако при неадекватном лечении рака начальных стадий этот тезис становится неоднозначным.
Все чаще больным ранним раком яичников пытаются выполнять «щадящие» операции (лапароскопические, роботические). Однако объём хирургического лечения всегда должен оставаться одним и тем же.
Обратимся к клиническим рекомендациям:
При I–II стадиях заболевания при ревизии органов брюшной полости выполняют все процедуры хирургического стадирования, а именно:
- Срединная лапаротомия для полноценной ревизии органов. Лапароскопическая хирургия при раке яичников I стадии возможна, но только при неукоснительном выполнении всех процедур стадирования.
- Если подтверждения диагноза злокачественной опухоли нет, то следует проводить срочное интраоперационное гистологическое исследование.
- Проведение цитологического исследования асцитической жидкости или смывов с брюшины.
- Все отделы брюшной полости, малого таза, включая поддиафрагмальное пространство, большой и малый сальник, тонкую и толстую кишку и их брыжейки, поверхность париетальной и висцеральной брюшины, забрюшинное пространство, тщательно и методично осматривают, все участки брюшины и спайки, подозрительные в отношении метастазов, подвергают биопсии.
- Если проведенная ревизия не выявила метастазов, выполняют биопсию случайно выбранных участков брюшины (в 8 точках).
- Удаление большого сальника выполняется на уровне большой кривизны желудка.
- Тотальная тазовая и поясничная лимфаденэктомия до уровня почечных сосудов.
Часто, не удалив большую часть парааортальных лимфоузлов, хирурги отправляют пациенток на химиотерапию. Такая тактика ухудшает прогноз.
При невыполнении ВСЕХ процедур стадирования при раке яичников ранних стадий целесообразно повторное хирургическое вмешательство с целью рестадирования. Химиотерапию важно начинать только после выполнения полноценной операции.
Хирургическое лечение первичного рака яичников III—IV стадий
Поздние стадии рака яичников не оставляют вариантов, поэтому хирургическое лечение проводят максимально агрессивно.
Во время операции, в идеале выполняемой ДО химиотерапии, важно стремиться к выполнению полной или оптимальной циторедукции. В противном случае все риски, которые влечёт за собой хирургическое лечение, напрасны.
Объем операции включает удаление всей видимой опухоли. При этом удаляются не только матка, маточные трубы и яичники, а также большой сальник, пораженная брюшина малого таза, брюшной полости, куполов диафрагмы, опухолевые диссеминаты.
Любая хирургическая операция сопряжена с риском осложнений. Чем больше объем удаляемых органов и тканей, тем этот риск выше. Его следует заранее обсудить с вашим хирургом.
В зависимости от распространения опухоли и глубины поражения тканей может потребоваться удаление и других органов, например резекция печени, части кишечника, поджелудочной железы, удаление желчного пузыря, селезенки, червеобразного отростка.
При удалении части толстой кишки ее иногда выводят на переднюю брюшную стенку, то есть формируют стому. В этом случае выделение кала происходит в герметично приклеенный к передней брюшной стенке мешочек — калоприемник. Стомы обычно выводят на какое-то время, реже они остаются навсегда.
Тем не менее, достижение полной или оптимальной циторедукции достоверно увеличивает вероятность излечения, время до прогрессирования, продолжительность жизни.
Сроки проведения химиотерапии после хирургического лечения
Зачастую онкологические пациенты существуют внутри системы: им дают направление, определяют лечение, а дальше процесс встает на паузу, потому что, например, нет квот, надо ехать в другой город и т.д. Но в реальной мировой практике химиотерапия проводится в жестко фиксированные сроки.
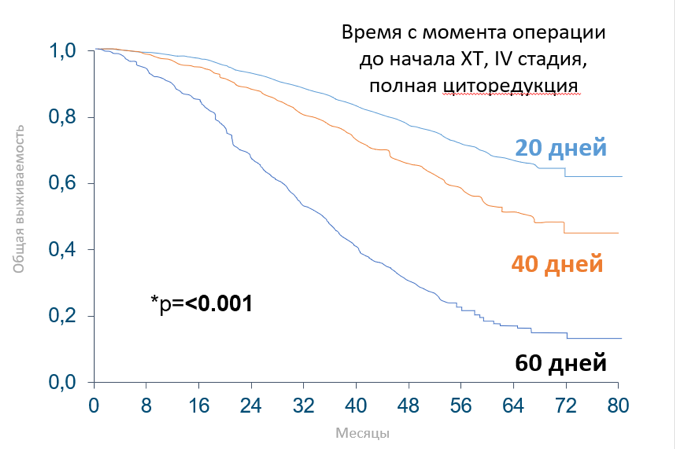
После полной первичной циторедукции химиотерапию важно начать в срок до 25 дней. Отсрочка начала химиотерапии снижает выживаемость.
Таким образом, послеоперационный период должен пройти максимально гладко, чтобы организм успел восстановиться перед химиотерапией.
Это возможно? С уверенностью скажем - да. Оцените сами статистику Health-Direct:
- частота послеоперационных осложнений 3-4 степени составляет менее 10%;
- средний койко-день в отделении реанимации —1;
- средний срок пребывания в стационаре после операции - 7 дней.
И это не результат применения современных методик fast-track, а реальные цифры после длительных травматичных операций с мультиорганными резекциями. Пациенты выписываются из клиники с хорошим настроением и самочувствием, а также со стабильными показателями анализов крови. В таком состоянии дома пациенты быстрее восстанавливаются перед химиотерапией и легче переносят специфическое противоопухолевое лечение.
Именно профилактика осложнений раннего послеоперационного периода, максимально быстрая активизация, раннее энтеральное питание и прочие принципы составляют основу стратегии лечения в Health-Direct.
Лечение с командой Health-Direct даёт вам не только уверенность в хирурге, но и в высокопрофессиональных анестезиологах и реаниматологах с колоссальным опытом ведения онкологических пациентов после расширенных и комбинированных хирургических вмешательств.
Современные подходы к интенсивной терапии, спланированная стратегия лечения, индивидуальный подход к каждому пациенту позволили нам добиться результатов, которые демонстрируют только ведущие онкологические центры мира.
Как проводится химиотерапия?
Золотой стандарт 1-й линии лечения рака яичников во всем мире — комбинация таксанов и препаратов платины. Чаще всего назначаются паклитаксел и карбоплатин. На выбор препаратов и режима их введения могут повлиять возраст и общее состояние здоровья.
Большинство препаратов при раке яичников вводят внутривенно, то есть лекарства вводят прямо в кровь через вену. Обычно пациенту устанавливают венозный порт для химиотерапии. Порт представляет собой небольшой круглый диск, который чаще всего размещают на грудной стенке. Его устанавливают во время небольшой операции и используют в течение всех курсов химиотерапии.
Препараты также могут вводить в брюшную полость. В этом случае процедура называется внутрибрюшинной химиотерапией. При таком способе введения более высокие дозы препаратов доставляются непосредственно к опухолевым клеткам рак. Химиотерапию проводят через внутрибрюшинную порт-систему. Ее устанавливают в конце операции при выполнении полной или оптимальной циторедукции.
Резюме
Лечение рака яичников – это взаимодействие пациентки и большой команды врачей. Именно пациентка в конечном итоге, учитывая все риски, определяет для себя оптимальный и приемлемый план лечения. Всегда следует обсуждать план лечения с несколькими экспертами, занимающимися лечением рака яичников (получать «второе мнение»).
Вопросы, которые необходимо обсудить с командой специалистов, занимающихся лечением рака яичников до принятия решения о плане лечения:
- Могу ли я рассчитывать на операцию на первом этапе? Если нет, почему?
- Как мой возраст, общее состояние здоровья и другие факторы влияют на выбор тактики лечения?
- Что делать, если я беременна или планирую беременность в будущем?
- Понадобится ли мне химиотерапия после операции?
- Учитываете ли вы зарубежные клинические рекомендации при рассмотрении вариантов лечения?
- Есть ли у меня возможность войти в клиническое испытание?
- Что происходит после лечения? Насколько вероятно, что у меня не будет рецидива?
- Какие побочные эффекты вызывает это лечение? Как они будут проявляться?
- Каковы шансы, что у меня появится другая злокачественная опухоль?
- Является ли лечение рака яичников вашей основной деятельностью?
- Какой процент тяжелых осложнений у вашей команды/вашей клиники? Какие?
- Каков опыт членов вашей команды?
Список литературы: / Для создания текста использовались следующие источники:
- Каприн А.Д., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2018г. (заболеваемость и смертность). М.: МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России, 2019. 250 с.
- Stewart C, Ralyea C, Lockwood S. Ovarian Cancer: An Integrated Review. Semin Oncol Nurs., 2019 Apr;35(2):151-156. doi: 10.1016/j.soncn.2019.02.001.
- Tewari KS, Java JJ, Eskander RN, Monk BJ, Burger RA. Early initiation of chemotherapy following complete resection of advanced ovarian cancer associated with improved survival: an NRG Oncology/Gynecologic Oncology Group study. Ann Oncol 2016;27(1):114–121
- Тюляндина А.С., Коломиец Л.А., Морхов К.Ю., Нечушкина В.М., Покатаев И.А., Румянцев А.А. и соавт. Практические рекомендации по лекарственному лечению рака яичников, первичного рака брюшины и рака маточных труб. Злокачественные опухоли : Практические рекомендации. RUSSCO #3s2, 2021 (том 11). 10
- Santotoribio J.D., Garcia-de la Torre A., Cañavate-Solano C. et al. Cancer antigens 19.9 and 125 as tumor markers in patients with mucinous ovarian tumors // Eur J Gynaecol Oncol. – 2016. – V. 37. – N 1. – P. 26–9
- Ledermann J. A., Raja F. A., Fotopoulou C. et al. Newly Diagnosed and Relapsed Epithelial Ovarian Carcinoma: ESMO Clinical Practice Guidelines // Ann Oncol. – 2013. –V. 24 (Suppl 6). – P. vi24–vi32.
- Harter P., Sehouli J., Lorusso D. et al. A Randomized Trial of Lymphadenectomy in Patients with Advanced Ovarian Neoplasms // N Engl J Med. – 2019. – V. 380. – P. 822– 832.
- Huo Y. R. et al. Hyperthermic intraperitoneal chemotherapy (HIPEC) and cytoreductive surgery (CRS) in ovarian cancer: a systematic review and meta-analysis //European Journal of Surgical Oncology (EJSO). – 2015. – Т. 41. – №. – С. 1578-1589.
- Elattar A. et al. Optimal primary surgical treatment for advanced epithelial ovarian cancer //Cochrane database of systematic reviews. – 2011. – №. 2А
- Yang L. et al. Neoadjuvant chemotherapy versus primary debulking surgery in advanced epithelial ovarian cancer: A meta-analysis of peri-operative outcome //PloS one. – 2017. – Т. 12. – №. – С. e0186725.
- Colombo N., Peiretti M., Garbi A. et al. Non-Epithelial Ovarian Cancer: ESMO Clinical Practice Guidelines // Ann Oncol. – 2012. – V. 23 (Suppl 7). – P. vii20–vii26